Представляем очередной выпуск нашего обновленного дайджеста FDA. В нем — уникальная подборка новостей по статусам Breakthrough therapy designation, присвоенным американским регулятором за март. Читайте нас и будьте в курсе самых последних инноваций в фармацевтике.

Новый препарат от атаксии Фридрейха (АФ) получил статус Breakthrough Therapy Designation.
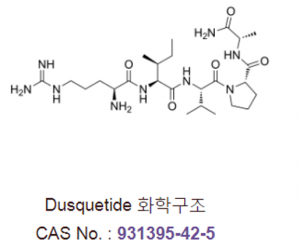
Nomlabofusp (ранее известный как CTI-1601) — это экспериментальный рекомбинантный гибридный белок, разработанный компанией Larimar Therapeutics в качестве потенциального средства, изменяющего течение атаксии Фридрейха (АФ). Он предназначен для устранения основного дефицита белка фратаксина у пациентов с АФ путем доставки человеческого фратаксина непосредственно в митохондрии.
Атаксия Фридрейха — наиболее частая наследственная атаксия (50% всех случаев), распространенность составляет 1 случай на 22 000 – 100 000 человек (чаще 1:40 000–50 000). Заболевание имеет аутосомно-рецессивный тип, проявляется обычно в 8–15 лет. Средняя продолжительность жизни часто составляет 40–50 лет, при этом ~50% пациентов не доживают до 35 лет.
АФ вызывается генетической мутацией, приводящей к низкому уровню митохондриального белка фратаксина. Номлабофусп — это гибридный белок, состоящий из клеточно-проникающего пептида (КПП), прикрепленного к человеческому фратаксину. Эта структура позволяет ему пересекать клеточные мембраны и проникать в митохондрии, где КПП удаляется, оставляя функциональный, зрелый фратаксин.
Larimar Therapeutics готовится в ближайшее время подать заявку на ускоренное одобрение в FDA. Если все пойдет хорошо, компания Larimar планирует вывести препарат на рынок США к первой половине 2027 года.
Hemab Therapeutics получила статус Breakthrough Therapy Designation для препарата Sutacimig при тромбастении Гланцмана
Hemab Therapeuticsъ объявила, что FDA присвоило препарату Sutacimig статус «прорывной терапии» для предотвращения эпизодов кровотечения у пациентов с тромбастенией Гланцмана (ТГ). Sutacimig — биспецифическое антитело, вводимое подкожно. Одна его часть связывает и стабилизирует эндогенный фактор VIIa, а другая — связывается с TLT-1 на активированных тромбоцитах.
Тромбастения Гланцмана — редкое наследственное заболевание крови (аутосомно-рецессивное), с частотой встречаемости примерно 1 случай на 1 млн новорожденных, хотя в популяциях с близкородственными браками этот показатель выше. Болезнь поражает мужчин и женщин одинаково часто, характеризуясь дефицитом тромбоцитарного рецептора GPIIb/IIIa. это тяжелое нарушение свертываемости крови, отличающееся изнурительными, иногда угрожающими жизни эпизодами кровотечений.
Механизм действия препарата способствует накоплению эндогенного фактора VIIa в организме и его непосредственному перемещению на поверхность активированных тромбоцитов, где он способствует образованию гемостатической пробки. Sutacimig разработан как первое в своем классе профилактическое средство для лечения тромбастении Гланцмана (ТГ) с потенциалом применения и для лечения других тяжелых нарушений свертываемости крови.
Ранее FDA присвоило Sutacimig статус ускоренного рассмотрения (Fast Track Designation) и статус орфанного препарата (Orphan Drug Designation) для лечения ТГ, а Агентство по регулированию лекарственных средств и медицинских изделий Великобритании (MHRA) присвоило сутацимигу статус орфанного лекарственного препарата в рамках инновационного пути лицензирования и доступа (ILAP). Sutacimig имеет потенциал стать первым в своем классе профилактическим средством для лечения тромбастении Гланцмана, наследственного серьезного нарушения свертываемости крови.
FDA присвоило препарату Sanofi статус Breakthrough Therapy Designation для лечения болезни Гоше
Venglustat (Ibiglustat) получил статус «прорывной терапии» от FDA на основании данных исследования LEAP2MONO, в котором у пациентов, получавших препарат, наблюдалось статистически значимое улучшение неврологических симптомов по сравнению с теми, кто получал ферментозаместительную терапию (имиглюцеразу).
Препарат в целом хорошо переносился, новых сигналов безопасности по сравнению с предыдущими исследованиями выявлено не было. Открытая фаза исследования продолжается, результаты будут представлены позже.
Болезнь Гоше — редкое наследственное заболевание (лизосомная болезнь накопления) с частотой встречаемости в общей популяции 1:40 000 – 1:70 000. Около 95% случаев составляет I тип (наиболее частый), 2 и 3 типы редки, их распространенность < 1 на 100 000 человек. Частота в популяции: 1 на 40 000 – 70 000 новорожденных. У евреев-ашкенази болезнь встречается значительно чаще — примерно у 1 из 450 человек.
Препарат действует за счет уменьшения аномального накопления глюкозфинголипидов (GSL) и предназначен для преодоления гематоэнцефалического барьера с целью воздействия на основную патологию неврологических эффектов.
Ранее Venglustat получил статус «ускоренного рассмотрения» и «орфанного препарата» для этого показания в США, Европейском Союзе и Японии.
Nia Therapeutics объявила о получении статуса «прорывного устройства» для своей интеллектуальной системы нейростимуляции (SNS)
Устройство с управлением на основе искусственного интеллекта использует классификаторы машинного обучения, обученные на сигналах мозга каждого пациента. Оно в режиме реального времени обнаруживает моменты нарушения кодирования памяти, а затем подает целенаправленную электрическую стимуляцию в латеральную височную кору. Устройство получило статус «прорывного устройства» для лечения эпизодической потери памяти у взрослых пациентов с перенесенной ранее черепно-мозговой травмой средней и тяжелой степени и стойкими нарушениями памяти.
Потеря памяти, часто вызванная деменцией, затрагивает более 57 млн человек в мире (2021 г.), причем 60-70% случаев — это болезнь Альцгеймера. Ежегодно выявляется около 10 млн новых случаев. У 40% людей старше 65 лет наблюдаются возрастные нарушения памяти, но лишь у 1% из них развивается деменция ежегодно. Помимо болезни Альцгеймера, память ухудшается из-за сосудистых заболеваний, травм, стресса и нейродегенеративных процессов.
Память зависит от скоординированной активности в обширных сетях головного мозга, поэтому создано устройство, которое может воспринимать и реагировать по всей сети. Благодаря 60 каналам в четырех областях мозга, система SNS обеспечивает улучшение на порядок по сравнению с уже одобренными устройствами DBS. Согласно пресс-релизу, SNS стала первым устройством, получившим статус «прорывного устройства» для лечения потери памяти, связанной с черепно-мозговой травмой.
Компания заявляет, что в настоящее время не существует одобренных FDA методов лечения потери памяти.
Источник: https://www.massdevice.com/nia-therapeutics-fda-breakthrough-nod-neuromod/