Jazz Pharmaceuticals сообщает о результатах КИ фазы II препарата для лечения посттравматического стрессового расстройства
Ирландская биофармацевтическая компания Jazz Pharmaceuticals plc объявила о результатах клинического исследования (КИ) фазы 2, где оценивалась эффективность и безопасность JZP150 — низкомолекулярного селективного ингибитора амидгидролазы жирных кислот (fatty acid amide hydrolase, FAAH) у взрослых с посттравматическим стрессовым расстройством (post-traumatic stress disorder, PTSD). Препарат не достиг поставленных целей. На этом фоне акции Jazz Pharmaceuticals потеряли 2,2% на внебиржевых торгах.

С начала года акции Jazz потеряли 26,6% по сравнению с падением отрасли на 4,4%.
Статистически значимого снижения общей тяжести симптомов посттравматического стрессового расстройства по шкале CAPS-5, при приеме JZP150 (4 мг или 0,3 мг) по сравнению с плацебо, от исходного уровня до 12-й недели не наблюдалось. КИ также не соответствовало ключевым критериям изменения вторичных конечных точек – от исходного уровня до 12-й недели по шкалам клинического общего впечатления о тяжести Clinical Global Impression of Severity, CGI-S) и общего впечатления пациента от тяжести (Patient Global Impression of Severity, PGI-S).
«Мы глубоко признательны всем, кто сделал это исследование возможным, и поддержал его, включая пациентов-участников, их семьи, наших ученых-исследователей и персонал исследования», — заявил Роб Ианноне (Rob Iannone), доктор медицины, исполнительный вице-президент, руководитель глобального отдела исследований и развития Jazz Pharmaceuticals. «Мы планируем полностью оценить эти данные, однако, основываясь на основных результатах, мы не ожидаем продолжения дополнительных разработок JZP150 для лечения PTSD. Мы признаем значительную неудовлетворенную потребность пациентов с PTSD и планируем в будущем поделиться с медицинским сообществом результатами этого исследования».
Никаких новых сигналов безопасности для JZP150 обнаружено не было. Наиболее частыми нежелательными явлениями (treatment emergent adverse events, TEAEs), возникшими во время лечения, были головная боль, тошнота и инфекция мочевыводящих путей. Они были преимущественно легкой или умеренной степени тяжести, а также встречались у участников, принимавших плацебо.
Еще одна компания, добившаяся обнадеживающих успехов в лечении PTSD, — это австралийская Binomics BNOX. Ранее в сентябре Binomics опубликовала основные данные КИ ATTUNE фазы II, оценивающего ведущего кандидата BNC210 в качестве потенциального средства лечения PTSD. Исследование ATTUNE достигло своей основной конечной точки — статистически значимого снижения общей тяжести симптомов посттравматического стрессового расстройства через 12 недель после лечения BNC210, измеренного по шкале CAPS-5. Bionomics намерена сотрудничать с FDA для обсуждения пути регистрации BNC210 при PTSD.

О JZP150
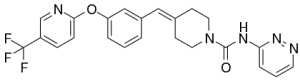
JZP150 (ранее PF-04457845) является ингибитором фермента гидролазы амидов жирных кислот (FAAH) с IC50 7,2 нМ, а его анальгезирующее и противовоспалительное действие в исследованиях на животных сравнимо с напроксеном.
JZP150 в настоящее время разрабатывается компанией Jazz Pharmaceuticals и проходит вторую фазу КИ в США для лечения посттравматического стрессового расстройства. Пациентам будут назначать 0,3 мг перорально один раз в день на срок до 12 недель или 4,0 мг перорально, 1 раз в день, на срок до 12 недель либо плацебо.
О клиническом исследовании JZP150 фазы 2
В многоцентровом двойном слепом плацебо-контролируемом рандомизированном КИ (NCT05178316) оценивались две дозы (4 мг и 0,3 мг) JZP150. В исследовании рандомизировали 282 взрослых в возрасте от 18 до 70 лет с диагнозом PTSD с использованием критериев «Диагностического и статистического руководства по психическим расстройствам Американской психиатрической ассоциации» (American Psychiatric Association’s Diagnostic and Statistical Manual for Mental Disorders), 5-е издание (DSM-5).
Первичная конечная точка исследования измеряла изменения участников от исходного уровня до 12-й недели с использованием общего балла CAPS-5, структурированного клинического интервью, которое считается золотым стандартом для диагностики и оценки пациентов с PTSD. Он включает в себя 30 пунктов, с помощью которых врачи могут поставить диагноз посттравматического стрессового расстройства и оценить тяжесть симптомов, а также их влияние на общее качество жизни. В исследовании было несколько вторичных конечных точек, включая изменения в баллах по шкале CGI-S и PGI-S.

О компании Jazz Pharmaceuticals plc
Jazz Pharmaceuticals plc (NASDAQ: JAZZ) — биофармацевтическая компания, базирующаяся в Ирландии, основанная в 2003 году слиянием Jazz Pharmaceuticals, Inc. и Azur Pharma plc. Одним из значительных продуктов компании является одобренный FDA препарат Xyrem (оксибат натрия), натриевая соль природного нейротрансмиттера γ-гидроксимасляной кислоты (ГОМК). В 2017 году чистый объем продаж продукции Xyrem был равен $1,187 млрд, что составило 74% от общего объема чистых продаж продукции компании.
В 2019 году Jazz получила одобрение FDA на продажу препарата Sunosi для лечения чрезмерной дневной сонливости (excessive daytime sleepiness, EDS) при нарколепсии, а также обструктивного апноэ во сне (obstructive sleep apnea OSA). В 2022 году было объявлено, что Axsome Therapeutics приобретет Sunosi у Jazz Pharmaceuticals.
Штаб-квартира Jazz находится в Дублине, Ирландия, а ее сотрудники работают по всему миру и обслуживают пациентов почти в 75 странах. Основные бренды: Xyrem, Erwinaze, Defitelio, FazaClo, FazaClo HD, Luvox CR, Prialt, Vyxeos и др.
Источник: https://pipelinereview.com/
Источник: https://finance.yahoo.com/
25.12.2023