FDA отказалась одобрить опиоидный препарат для лечения депрессии
Американские регуляторы отказали в регистрации экспериментальному препарату ALKS 5461, разработанному компанией Alkermes для лечения клинической депрессии у пациентов, не ответивших на терапию стандартными средствами. Как пишет Reuters, это уже второй отказ FDA в регистрации препарата.
Buprenorphine/samidorphan
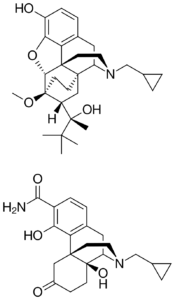
ALKS 5461 является комбинированным лекарственным препаратом для приема внутрь на основе бупренорфина и самидорфана – экспериментального селективного антогониста опиоидных рецепторов подтипа мю-. Бупренорфин является частичным агонистом опиоидных рецепторов подтипа мю- и антагонистом каппа-рецепторов. В настоящее время бупренорфин одобрен в ряде стран (в том числе в РФ) в качестве опиоидного анальгетика.

Как и в прошлый раз, контрольные органы запросили дополнительную информацию, доказывающую эффективность ALKS 5461. В поддержку регистрационной заявки были предоставлены данные клинических исследований, прошедших при участии 407 пациентов, принимавших экспериментальное средство или плацебо. Все участники КИ продолжили стандартную терапию депрессии. Согласно полученным результатам, на фоне нового препарата у пациентов значительно сокращались проявления депрессии. При этом был отмечен благоприятный профиль безопасности лекарственного средства: наиболее распространенными побочными эффектами были тошнота, головокружение и усталость.
Источник: http://remedium.ru
6.02.2019