Американские регуляторы оказались быстрее европейских
Анализ работы контрольных органов США и ЕС выявил, что Администрация по контролю за продуктами и лекарствами США (FDA) работает быстрее, чем Европейское агентство по лекарственным средствам (EMA).
Результаты исследования были опубликованы в New England Journal of Medicine.

Исследователи из Йельского университета сравнили данные по деятельности двух контрольных органов за четыре года (2011-2015 гг.).
Оказалось, что за это время FDA зарегистрировала 170 лекарственных препаратов, а EMA – 144.
В пропорциональном соотношении американские регуляторы одобрили больше орфанных ЛС – 43,5% от всех зарегистрированных препаратов (в ЕС данный показатель составил только 25%).
Средняя продолжительность рассмотрения регистрационной заявки сотрудниками FDA составила 306 дней (от 239 до 371), работникам EMA на это требуется больше времени – в среднем 383 дня (от 327 до 446).
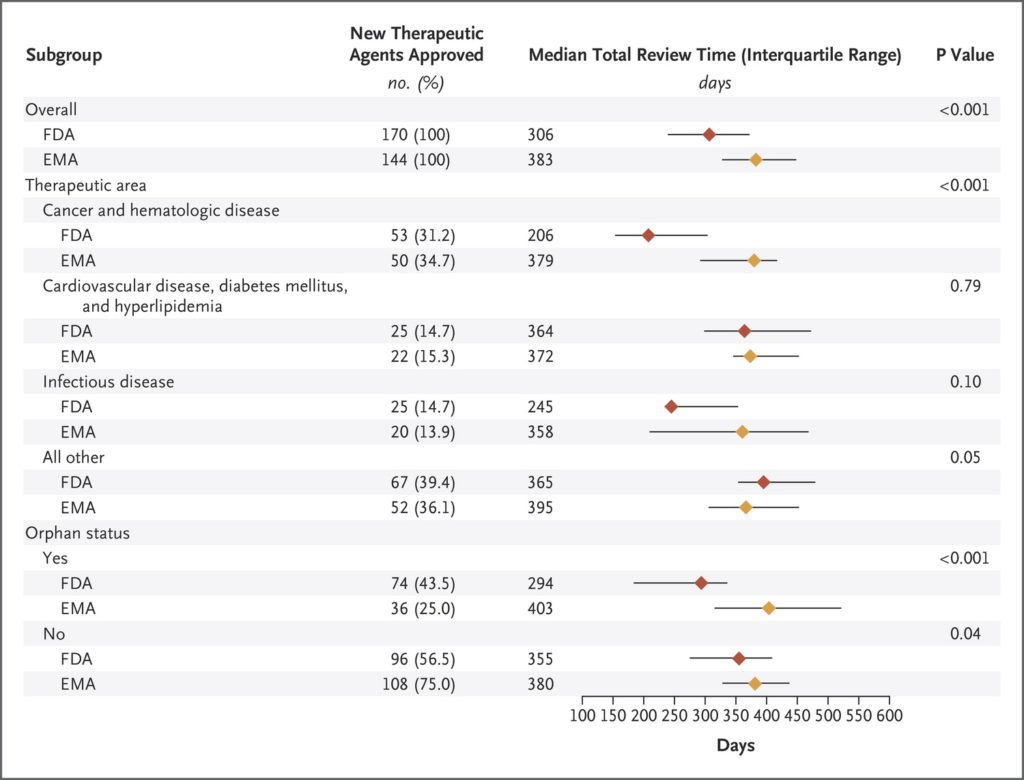
Median Total Review Time in Days for New Therapeutic Agents Approved by the Food and Drug Administration (FDA) or the European Medicines Agency (EMA) between 2011 and 2015.
Источник: N Engl J Med 2017; 376:1386-1387 April 6, 2017 — DOI: 10.1056/NEJMc1700103
В последнее время FDA подвергается критике за несовершенную и слишком продолжительную процедуру рассмотрения заявок на регистрацию новых лекарственных препаратов.
Ранее президент США Дональд Трамп пообещал фармкомпаниям ускорить и упростить процедуру вывода на рынок новых медикаментов.<br
Источник: http://remedium.ru
6.04.2017