Антисмысловые олигонуклеотиды обратили вспять редкое нейроразвивающее расстройство в доклинических моделях
Ученые из Детской исследовательской больницы Сент-Джуд (St. Jude Children’s Research Hospital) обнаружили возможность обратить вспять последствия нейроразвивающего расстройства, связанного с HNRNPH2, используя антисмысловые олигонуклеотиды (antisense oligonucleotides, АSО) в доклинических моделях. АSО — это короткие синтетические нити нуклеиновых кислот, нацеленные на специфическую матричную РНК.

В статье, опубликованной в журнале Science Translational Medicine, исследователи показали, что АSО блокируют выработку аберрантного белка HNRNPH2. Это, в свою очередь, усиливает экспрессию близкородственного белка HNRNPH1, уменьшая множество симптомов расстройства. Выполненное пионерское исследование предоставило важные данные о механизме действия, которые помогут продвинуть эту многообещающую терапию в клинические исследования.
Нейроразвивающее расстройство, связанное с HNRNPH2, — это Х-сцепленное генетическое заболевание, симптомы которого включают задержку развития и судороги, а также проблемы с двигательной функцией, обучением и памятью. На сегодняшний день зафиксировано менее 200 случаев недуга, что классифицирует его как ультраредкое заболевание. В настоящее время лекарства от него не существует, отчасти потому, что редкость этого состояния представляет собой препятствие как для исследований, так и для инвестиций в терапию.
«С тех пор, как 10 лет назад у пациентов было впервые выявлено расстройство, связанное с HNRNPH2, мы работали над тем, чтобы лучше понять механизмы, лежащие в основе заболевания. Замечательным совпадением стало то, что мы обнаружили его молекулярную основу как раз в тот момент, когда антисмысловые олигонуклеотиды (ASO) стали эффективной терапевтической технологией. Выявленный нами механизм особенно хорошо подходил для подхода на основе ASO, позволяя нам вмешиваться непосредственно в источник заболевания. Это исследование представляет собой следующий шаг к реальному облегчению страданий пациентов и их семей, для которых в настоящее время отсутствуют варианты лечения». — заявил Дж. Пол Тейлор (J. Paul Taylor), исполнительный вице-президент St. Jude и директор Инициативы по трансляционной нейробиологии в педиатрии (Pediatric Translational Neuroscience Initiative).
Терапия с использованием антисмысловых олигонуклеотидов (ASO) подавляет экспрессию белка HNRNPH2 и усиливает экспрессию очень близкого по структуре белка HNRNPH1.
Вместо изменения самого мутированного гена, терапия с использованием ASO нацелена на матричную РНК, продуцируемую этим геном. ASO, нацеленные на HNRNPH2, помечают его РНК для разрушения до того, как будет синтезирован аберрантный белок. Предыдущие исследования лаборатории Тейлора показали, что снижение уровня белка HNRNPH2 стимулирует экспрессию близкородственного белка HNRNPH1 для компенсации.
Оба белка жизненно важны для обработки РНК и, вероятно, играют перекрывающиеся роли в процессе развития. Примечательно, что в то время как экспрессия HNRNPH1 снижается по мере развития, экспрессия HNRNPH2 сохраняется до тех пор, пока клетки не станут все более зависимыми от него. Однако механизм, лежащий в основе этого перехода в развитии, и то, как HNRNPH2 влияет на экспрессию HNRNPH1, оставались неясными. Кроме того, исследователи не были уверены, приводят ли мутации HNRNPH2 к нарушению работы белка (усиление функции) или к его отсутствию (потеря функции).
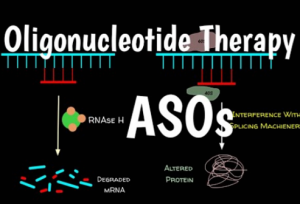
В этом исследовании ученые обнаружили, что HNRNPH2 регулирует экспрессию HNRNPH1, способствуя системам экспрессии генов пропускать важную часть гена. Этот пропуск приводит к немедленному удалению любой полученной мРНК HNRNPH1. Исследование показало, что подавление мутированного HNRNPH2 с помощью антисмыслового олигонуклеотида (ASO) может обратить этот пропуск вспять, что приводит к увеличению экспрессии HNRNPH1 и улучшению состояния пациентов.
«Мы предположили, что стратегия ASO, которая существенно снижает уровни HNRNPH2 и увеличивает экспрессию HNRNPH1, должна оказаться эффективной как для механизмов усиления функции, так и для механизмов потери функции, и улучшить симптомы в доклинических моделях HNRNPH2», — сказала первый автор Ане Корфф (Ané Korff), доктор философии, кафедра клеточной и молекулярной биологии Сент-Джуд. «Проведенное исследование проверяет эту идею».
«Мы обнаружили, что многие симптомы исчезали после неонатального лечения с помощью ASO в доклинических моделях, а также подтвердили этот эффект после лечения у детей старшего возраста», — добавила Корфф. Поскольку генетическая диагностика заболеваний, связанных с HNRNPH2, может занять несколько лет, этот результат предполагает, что терапия с использованием ASO может оказаться полезной даже в более позднем возрасте.
Полученные результаты предоставляют доклинические доказательства того, что стратегия с использованием ASO может кардинально изменить ситуацию с нейроразвивающими расстройствами, связанными с HNRNPH2, и с ультраредкими заболеваниями в целом. «Первые случаи этого расстройства были зарегистрированы в 2016 году, и за 10 лет мы перешли от фундаментальной биологии к разработке трансляционной терапии, которая потенциально способна оказывать реальное влияние на пациентов», — считает соавтор Хонг Джу Ким (Hong Joo Kim), доктор философии, сотрудник отдела клеточной и молекулярной биологии Сент-Джуд. «Это удивительное достижение, и очень важно, что работа быстро продвигается, чтобы помочь пациентам».
Антисмысловая терапия
Антисмысловая терапия (antisense therapy) — метод лечения, основанный на выключении/остановке синтеза белка, участвующего в развитии заболевания, путём ингибирования трансляции его матричной РНК с помощью комплементарных к ней коротких нуклеотидных последовательностей (антисмысловых олигонуклеотидов).
Об антисмысловых олигонуклеотидах
Антисмысловые олигонуклеотиды (АSО) — это короткие синтетические цепочки ДНК/РНК (16–20 нуклеотидов), блокирующие синтез болезнетворных белков путем связывания с матричной РНК. Они применяются для лечения редких (орфанных), неврологических и генетических заболеваний, включая спинальную мышечную атрофию (СМА) и мышечную дистрофию Дюшенна.
Основные зарегистрированные препараты:
- Нусинерсен (Спинраза): Применяется для лечения СМА, увеличивая выработку белка SMN.
- Этеплирсен (Exondys 51): Используется при мышечной дистрофии Дюшенна, восстанавливая синтез дистрофина.
- Мипомерсен (Kynamro): Применяется для снижения уровня холестерина при гомозиготной семейной гиперхолестеринемии.
- Во ihopersen (Waylivra): Предназначен для лечения семейного синдрома хиломикронемии.
Ключевые характеристики и направления:
- Механизм: Химически модифицированные АSО (для защиты от распада) связываются с целевой пре-мРНК, вызывая ее деградацию или меняя процесс сплайсинга.
- Применение: Эффективны при мышечных патологиях, нейродегенеративных заболеваниях (боковой амиотрофический склероз, синдром Драве).
- Разработка: Активно разрабатываются новые АСО для борьбы с антибиотикорезистентными инфекциями.
Препараты этого класса позволяют воздействовать на саму причину генетических болезней, а не только на симптомы.
Источник: https://www.news-medical.net/
Источник: https://medicalxpress.com/
27.04.2026