FDA одобрило экстренное использование Ремдесивира для лечения COVID-19
FDA в пятницу одобрило экспериментальный препарат ремдесивир для экстренного применения при лечения COVID-19 – спустя всего несколько дней после того, как предварительное исследование сообщило, что он сократил пребывание в стационаре для пациентов с COVID-19.
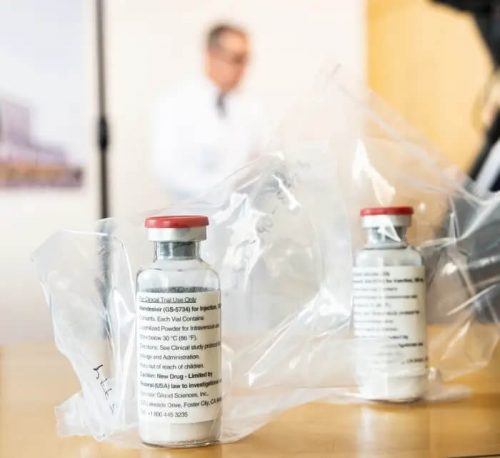
В заявлении о выдаче разрешения на экстренное использование главный научный сотрудник FDA Дениз Хинтон заключила: «Разумно полагать, что известные и потенциальные преимущества препарата ремдесивир перевешивают известные и потенциальные риски применения препарата для лечения пациентов, госпитализированных с тяжелой степенью COVID-19». Разрешение на лекарственное средство пришло через два дня после отчета о спонсируемом Национальным институте здоровья клиническом испытании (КИ). В эксперименте с 1063 пациентами, КИ показало, что, хотя препарат статистически не снижал смертность у пациентов с COVID-19, но медиана пребывания в стационаре составила 11 дней, а не 15 дней – для пациентов, получавших плацебо. Новости об одобрении пришли от президента Дональда Трампа – в пятницу, совместно с генеральным директором Gilead Sciences, компании-производителем препарата. Ремдесивир – противовирусный препарат, препятствующий размножению вирусов в клетках, первоначально предназначенный для лечения коронавирусов MERS и SARS. «Я думаю, что данное событие действительно иллюстрирует, что может произойти за такое короткое время», – заявила Дебора Биркс из целевой группы Белого дома по коронавирусу. Отдельное небольшое КИ ремдесивира на 237 пациентах, опубликованное в Lancet в среду, не выявило клинических преимуществ лечения пациентов с COVID-19 этим препаратом – его использование было остановлено, поскольку препарат вызывал более высокий процент побочных эффектов. Тем не менее, исследование показало аналогичные признаки сокращения пребывания в стационаре, хотя и не в статистически значимой степени. Оба исследования начались в феврале.
Источник: https://www.buzzfeednews.com/article/danvergano/fda-remdesivir-coronavirus
4.05.2020