FDA продлило рассмотрение препарата DNLI для лечения синдрома Хантера на три месяца
FDA продлило рассмотрение препарата DNLI – тивиденофусп альфа (tividenofusp alfa) компании Denali Therapeutics Inc. для лечения синдрома Хантера (Hunter Syndrome). Срок рассмотрения был перенесен регулятором с 5 января на 5 апреля 2026 года после того, как Denali представила новые фармакологические данные.

Продление не связано с безопасностью или эффективностью, и FDA не запрашивало никаких дополнительных данных. Denali Therapeutics Inc. (DNLI Quick Quote — Free Report) объявила, что FDA продлило срок рассмотрения заявки на получение лицензии на биологический препарат (Biologics License ApplicationBLA) для препарата-кандидата на разработку, tividenofusp alfa.
Denali Therapeutics Inc. добивается ускоренного одобрения препарата tividenofusp alfa для лечения мукополисахаридоза II типа (mucopolysaccharidosis type II, MPS II) I), также известного как синдром Хантера. Продление срока является неудачей для Denali, поскольку компания вынуждена откладывать возможное и ожидаемое одобрение своего основного препарата-кандидата на разработку. В связи с этим, акции Denali упали на внебиржевых торгах 13 октября, следует отметить, что акции DNLI потеряли 26,5% с начала года, в то время, как в целом, по отрасли рост составил 9,2%.
Нужно учитывать, что Denali представила обновленную информацию о клинической фармакологии в ответ на запрос регулирующего органа в рамках стандартной процедуры рассмотрения. Продление срока не связано с эффективностью, безопасностью или биомаркерами. В свою очередь, FDA классифицирует заявку как существенную поправку к BLA, в связи с чем срок рассмотрения был продлен.
Тем не менее, FDA не запрашивало никаких дополнительных данных, поэтому Denali обоснованно считает, что обновленная информация, представленная в поправке, не влияет на клиническую фармакологию или выводы BLA по соотношению пользы и риска.
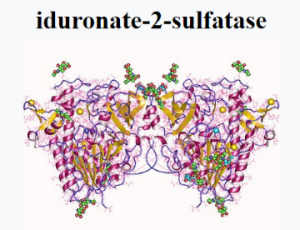
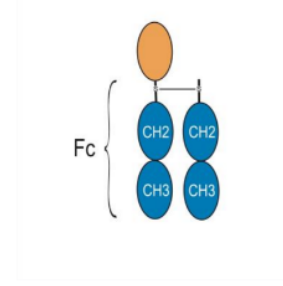
Тividenofusp alfa (DNL310) состоит из фермента идуронат-2-сульфатазы (iduronate 2-sulfatase, IDS), интегрированного с собственной платформой Denali TransportVehicle (TV). Препарат предназначен для доставки IDS в головной мозг и тело с целью устранения поведенческих, когнитивных и физических симптомов синдрома Хантера.
Ранее FDA предоставило tividenofusp alfa статусы Fast Track и Breakthrough Therapy Designations для разработки препарата для лечения МПС II. Европейское агентство по лекарственным средствам присвоило препарату статус «Приоритетное лекарственное средство» (Priority Medicines Designation). Исследование COMPASS II/III фазы проводит набор пациентов с МПС II в Северной Америке, Южной Америке и Европе для поддержки глобального одобрения. Тividenofusp alfa является экспериментальным препаратом и не одобрен к применению ни одним органом здравоохранения.
Другие перспективные кандидаты DNLI
Denali также изучает DNL126 для лечения синдрома Санфилиппо типа A (МПС IIIA). Ранее компания достигла соглашения с Центром оценки и исследований лекарственных средств FDA о том, что уровень гепарансульфата в спинномозговой жидкости (ГС СМЖ) может считаться достаточно вероятной суррогатной конечной точкой для прогнозирования клинической эффективности и, следовательно, может быть использован для ускоренного одобрения препарата DNL126 для лечения МПС IIIA.
Ещё одним кандидатом в портфеле DNLI является TAK-594/DNL593. Denali сотрудничает с Takeda в совместной разработке и коммерциализации DNL593 – терапевтического кандидата, предназначенного для доставки програнулина через ГЭБ в лизосомы для лечения лобно-височной деменции (ЛВД), связанной с мутацией в гене гранулина (GRN). Denali проводит исследование фазы I/II DNL593 при ЛВД-GRN.
Denali и Biogen (BIIB Quick QuoteBIIB — Free Report) совместно оценивают ингибитор LRRK2 BIIB122/DNL151, разрабатываемый для лечения болезни Паркинсона (БП). Biogen возглавляет глобальное исследование LUMA фазы IIb, оценивая влияние BIIB122 на прогрессирование заболевания на ранней стадии БП. В мае 2025 года Biogen объявила о полном наборе участников в исследование LUMA, результаты которого ожидаются в 2026 году. Тем временем Denali проводит исследование BEACON фазы IIa, в частности, набирая участников с БП, ассоциированной с LRRK2, чтобы оценить, как ингибирование LRRK2 может повлиять на это заболевание.
Denali планирует подавать заявки в регулирующие органы для начала клинических испытаний одной-двух телевизионных программ каждый год в течение следующих трёх лет в рамках своих франшиз Enzyme TV (ETV), Antibody TV (ATV) и Oligonucleotide TV (OTV).
Рейтинг Zacks и ключевые рекомендации
Акции Denali в настоящее время имеют рейтинг Zacks #3 (держать). В биотехнологическом секторе есть несколько более высоко оцененных акций: Amicus Therapeutics (FOLD Quick QuoteFOLD — бесплатный отчет) и CorMedix (CRMD Quick QuoteCRMD — бесплатный отчет). В то время как FOLD в настоящее время имеет рейтинг Zacks #1 (активная покупка), CRMD имеет рейтинг Zacks #2 (покупать).
За последние 60 дней прогноз прибыли на акцию (EPS) Amicus Therapeutics в 2025 году оставался неизменным на уровне 31 цента. Прогноз прибыли на акцию на 2026 год увеличился с 68 до 70 центов за тот же период. Прибыль Amicus Therapeutics превзошла прогнозы в одном из последних четырёх кварталов, но в остальных трёх случаях оказалась ниже ожидаемого уровня. Средний отрицательный показатель составил 24,38%.
За последние 60 дней прогноз прибыли на акцию CorMedix на 2025 год вырос с 1,22 до 1,85 доллара. За тот же период прогноз прибыли на акцию на 2026 год вырос с 2,12 до 2,49 доллара. С начала года акции CRMD выросли на 30,6%. Прибыль CorMedix превзошла прогнозы в каждом из последних четырёх кварталов, обеспечив средний отрицательный показатель в 34,85%.
О синдроме Хантера (MPS II)
Синдром Хантера, также известный как МПС II, — редкое генетическое лизосомное заболевание накопления, вызванное мутациями в гене идуронат-2-сульфатазы (IDS). Это приводит к дефициту фермента ИДС, который отвечает за расщепление гликозаминогликанов (ГАГ), таких как гепарансульфат и дерматансульфат. Накопление ГАГ приводит к прогрессирующему повреждению множества органов и тканей, включая головной мозг. Симптомы синдрома Хантера включают задержку развития, снижение когнитивных функций, поведенческие отклонения и физические осложнения, такие как скованность суставов, потеря слуха и дисфункция органов. Современные стандартные методы заместительной ферментной терапии не проникают через гематоэнцефалический барьер и, следовательно, не устраняют неврологические симптомы заболевания. Существует значительная неудовлетворенная потребность в методах лечения, которые воздействуют как на центральную нервную систему (ЦНС), так и на периферические проявления синдрома Хантера.
О компании Denali Therapeutics
Denali Therapeutics — созданная в 2015 году биотехнологическая компания, разрабатывающая широкий портфель препаратов-кандидатов, способных преодолевать гематоэнцефалический барьер (ГЭБ) для лечения нейродегенеративных заболеваний и лизосомных болезней накопления. Denali разрабатывает новые методы лечения, тщательно оценивая генетически подтвержденные мишени, разрабатывая способы доставки препаратов через ГЭБ и направляя разработки на основе биомаркеров, демонстрирующих взаимодействие с мишенями и сигнальными путями. Компания Denali расположена в Южном Сан-Франциско.
Источник: https://www.zacks.com/
Источник: https://www.linkedin.com/
Источник: https://www.denalitherapeutics.com/
15.10.2025