Gyre Pharmaceuticals завершила набор участников в исследование фазы III препарата Pirfenidone при пневмокониозе
Американская биофармацевтическая компания Gyre Pharmaceuticals завершила набор участников в 52-недельное клиническое исследование III фазы препарата Pirfenidone (в капсулах) для лечения пневмокониоза. В рандомизированном многоцентровом плацебо-контролируемом двойном слепом исследовании, проводимом в 18 клинических исследовательских центрах Китая, примут участие 272 человека.

Цель исследования — оценить безопасность и эффективность лечения Pirfenidone в капсулах у пациентов с хроническим профессиональным заболеванием лёгких — пневмокониозом, характеризующимся прогрессирующим легочным фиброзом.
В исследовании будет оцениваться эффективность капсул в суточной дозе 1800 мг (по 600 мг 3 раза в день) в сравнении с плацебо в течение 52 недель. Первичная конечная точка фокусируется на изменении процентного показателя прогнозируемой форсированной жизненной ёмкости лёгких на 52-й неделе по сравнению с исходным уровнем.
Ключевые вторичные конечные точки включают изменения диффузионной способности лёгких по угарному газу, оценку по респираторному опроснику больницы Святого Георгия, дистанцию шестиминутной ходьбы и шкалу одышки, а также показатели смертности, острых обострений и госпитализаций.
Мониторинг безопасности основан на обновленном отчете Gyre по безопасности разработки, охватывающем период с декабря 2023 года по декабрь 2024 года. Большинство зарегистрированных нежелательных явлений классифицируются как легкие или умеренные, непредвиденных сигналов безопасности не выявлено.
Pirfenidone — пероральный антифибротический препарат с «малой» молекулой, одобренный компанией Gyre Pharmaceuticals в Китае в 2011 году для лечения идиопатического легочного фиброза. Этот препарат действует путем ингибирования сигналов TGF-β и пролиферации фибробластов.

Пневмокониоз остается самым распространенным профессиональным заболеванием в стране, поражая более 450 000 человек, и ежегодно регистрируются тысячи новых случаев. Это заболевание возникает в результате длительного вдыхания минеральной пыли, такой как кремний и уголь, что приводит к прогрессирующему фиброзу и хроническому воспалению легочной ткани.
Исследования, проводимые компанией Gyre Therapeutics
Gyre Therapeutics — биофармацевтическая компания со штаб-квартирой в Сан-Диего (Калифорния), в первую очередь, занимающаяся разработкой и коммерциализацией в США препарата Hydronidone (F351) для лечения стеатогепатита, связанного с метаболической дисфункцией (фиброза печени, связанного с MASH, «фиброз MASH»), ранее известного как неалкогольный стеатогепатит (НАСГ). Hydronidone в настоящее время изучается для лечения фиброза печени – при широком спектре хронических заболеваний печени в рамках активной заявки на исследование нового лекарственного препарата (IND). Эта IND подкреплена комплексной доклинической программой, соответствующей требованиям GLP, и клиническим исследованием фазы 1 данных по фармакокинетике, безопасности и переносимости однократных и многократных возрастающих доз Hydronidone у здоровых добровольцев в США. Расширение показаний к применению препарата MASH основано на результатах механистических исследований на модели грызунов MASH и, что более важно, на результатах клинического исследования фазы 2, проведенного в Китае при хроническом фиброзе печени, вызванном гепатитом B, которое достигло первичных конечных точек безопасности и эффективности и недавно привело к признанию препарата прорывным в терапии Управлением по новым лекарственным препаратам Китая (NMPA).
Помимо показаний к применению препарата MASH в США, Gyre также развивает широкий спектр препаратов – Pirfenidone, F573, F528 и F230. Pirfenidone, одобренный в Китае препарат для лечения идиопатического легочного фиброза, в настоящее время проходит клинические испытания фазы 3 при дерматомиозите, интерстициальном заболевании легких, связанном с системной склеродермией, и пневмокониозе, а также клинические испытания фазы 1 при диабетической болезни почек. Препарат F573 в настоящее время изучается при острой печеночной недостаточности на фоне хронической, а F528 и F230 — при хронической обструктивной болезни легких и легочной артериальной гипертензии, соответственно.
О пневмокониозе
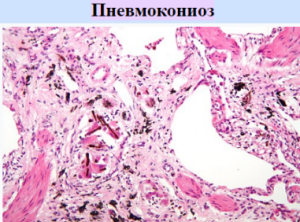
Пневмокониоз (лат. pneumon — лёгкие и konia — пыль) — группа заболеваний лёгких человека (необратимых и неизлечимых), вызванных накоплением в лёгких достаточно большой дозы нерастворимой производственной пыли, вызывающей развитие в них фиброзного процесса. Пневмокониозы относятся к профессиональным болезням. Начальные стадии не выявляются при флюорографии и могут быть обнаружены при вскрытии при вредном стаже менее 1 года. Встречаются у рабочих горнорудной, угольной, машиностроительной и некоторых др. отраслей промышленности.
Формы пневмокониоза – Антракоз: угольщиков (легкие шахтера); Сиккоз: От вдыхания частиц кварца; Талькоз: От вдыхания пыли талька.
В 2013 году пневмокониозы стали причиной 260 000 смертей во всем мире, по сравнению с 251 000 смертями в 1990 году. Из этого числа 46 000 смертей произошли из-за силикоза, 24 000 — из-за асбестоза и 25 000 — из-за пневмокониоза у работников угольной промышленности.
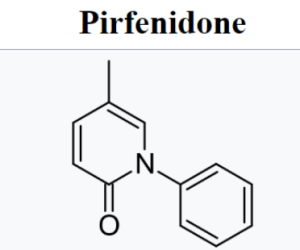
О препарате Pirfenidone
Pirfenidone, продающийся, в частности, под торговой маркой Pirespa, — препарат, применяемый для лечения идиопатического легочного фиброза. Он уменьшает фиброз легких за счет снижения выработки факторов роста и проколлагенов I и II. Впервые он был одобрен в Японии для лечения пациентов с идиопатическим легочным фиброзом после клинических испытаний в 2008 году. Препарат также был одобрен для применения в Европейском союзе в 2011 году, в Канаде — в 2012 году, а в США — в октябре 2014 года. Он доступен в виде дженерика.
Источник: https://www.clinicaltrialsarena.com/
Источник: https://www.linkedin.com/
Источник: https://www.gyretx.com/about/
17.10.2025