Исследователи определили ключевого игрока в клеточном ответе на стресс
Новое исследование показало, что фермент под названием Fic, биохимическая роль которого была открыта в научно-исследовательском медицинском центре UT Southwestern (UTSW) более десятка лет назад, играет решающую роль в управлении клеточным ответом на стресс. Результаты, опубликованные в журнале PNAS, могут в конечном итоге привести к появлению принципиально новых методов лечения различных заболеваний.

«Мы считаем, что Fic действует как термостат, регулирующий реакцию клетки на стрессовые факторы. Если получится взять этот термостат под контроль и настроить его в разных тканях должным образом, мы в дальнейшем сможем замедлить либо даже остановить прогрессирование некоторых заболеваний», — сказала Аманда Кейси (Amanda Casey), доктор философии, профессор кафедры молекулярной биологии. Кейси руководила проведенным исследованием вместе с Ким Орт (Kim Orth), доктором философии, профессором молекулярной биологии Медицинского института Говарда Хьюза (Howard Hughes Medical Institute).
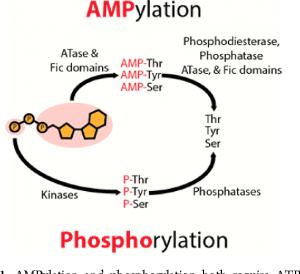
Первоначально обнаруженный в бактериях Vibrio parahaemolyticus, которые, как известно, вызывают пищевое отравление, Fic долгое время был в центре внимания лаборатории Ким Орт. В 2009 году доктор Орт и ее коллеги опубликовали первую статью, показывающую, что Fic участвует в процессе, называемом AMPylation, в котором этот фермент облегчает перенос фосфатной и аденозиновой групп на другие белки, изменяя их активность. Вскоре исследователи обнаружили, что животные, от червей до людей, также имеют фермент Fic.
Исследования на плодовых мушках показали, что Fic, по-видимому, важен для устойчивости к стрессу и восстановления. В статье, опубликованной в 2018 году доктором Орт и доктором Гельмутом Кремером (Helmut Krämer), доктором философии, профессором нейробиологии и клеточной биологии UTSW, и их коллегами показано, что мухи, постоянно подвергающиеся воздействию яркого света, который повреждает их глаза, получают необратимый вред, если их ген Fic был удален с помощью генной инженерии. Однако роль этого фермента у млекопитающих была неясна.

Ким Орт (Kim Orth)
Чтобы ответить на этот вопрос, исследователи создали модель мыши без гена Fic. Эти животные изначально были неотличимы от однопометников с Fic, и казались здоровыми. Однако, когда исследователи не кормили животных в течение 14 часов, а затем позволяли им есть столько, сколько они хотели, мыши ели в течение двух часов, что является стрессом для поджелудочной железы, контролирующей уровень сахара в крови и вырабатывающей ключевые пищеварительные ферменты. При этом, животные с дефицитом Fic показали гораздо более высокую реакцию на стресс, чем животные с Fic. Дальнейшее исследование показало, что молекулярный путь, называемый реакцией развернутого белка (unfolded protein response, UPR), который активируется, когда клетки в стрессовом состоянии не могут справиться со складыванием вновь генерируемых белков, намного сильнее активирован у животных с дефицитом Fic.

Аманда Кейси (Amanda Casey)
Исследователи сделали аналогичные выводы, когда мышам вводили препарат под названием церулеин, действующий на поджелудочную железу, вызывая повышенный выброс пищеварительных ферментов. Интересно, что хотя животные с Fic быстро выздоравливали, у тех, кто не имел Fic, в поджелудочной железе образовывались необратимые рубцы — признак значительно более низкой устойчивости к стрессу.
Доктор Орт добавила, что неконтролируемая клеточная реакция на стресс и реакция развернутого белка играют роль во многих заболеваниях, включая рак, метаболический синдром, атеросклероз, дегенерацию сетчатки и различные нейродегенеративные расстройства. «Если мы сможем определить, как устроен этот «стрессовый термостат», то, конечно, сможем повысить либо понизить его при различных заболеваниях, где стрессовая реакция является знаковым фактором», — отметила она.
Среди других исследователей UTSW, которые внесли свой вклад в это исследование, были Хиллери Ф. Грей, Сунита Чималапати, Хенаро Эрнандес, Эндрю Мелман, Натан Стюарт, Хейзел А. Филдс, Бурак Гюлен, Келли А. Серваж, Каролина Стефаниус, Обри Блевинс, Брет Эверс и Хельмут. Крамер.
Исследование финансировалось за счет грантов Фонда Уэлча (I-1561), Фонда «Однажды в сказке», Национальных институтов здравоохранения (R35 GM130305 и EY10199) и стипендии Фонда исследований в области наук о жизни.
Доктор Орт руководит кафедрой биомедицинских наук имени Эрла А. Форсайта и является научным сотрудником в области биомедицинских исследований Фонда W.W. Карута-младшего (W.W. Caruth, Jr.). Она также является членом Комплексного онкологического центра Гарольда С. Симмонса (Harold C. Simmons Comprehensive Cancer Center).
Материалы предоставлены: UT Southwestern Medical Center.
Публикация:
Amanda K. Casey, Hillery F. Gray, Suneeta Chimalapati, Genaro Hernandez, Andrew T. Moehlman, Nathan Stewart, Hazel A. Fields, Burak Gulen, Kelly A. Servage, Karoliina Stefanius, Aubrie Blevins, Bret M. Evers, Helmut Krämer, Kim Orth. Fic-mediated AMPylation tempers the unfolded protein response during physiological stress. Proceedings of the National Academy of Sciences, 2022; 119 (32) DOI: 10.1073/pnas.2208317119.
Источник: https://www.sciencedaily.com/
4.10.2022