J&J получает Fast Track Designation для Nipocalimab против умеренной и тяжелой формы болезни Шегрена
Johnson & Johnson объявила, что FDA предоставило Nipocalimab статус Fast Track Designation (FTD) для лечения взрослых пациентов с болезнью Шегрена (Sjögren‘s Disease, SjD) средней и тяжелой степени. В конце прошлого года препарат получил статус Breakthrough Therapy (BTD). В настоящее время для лечения этого заболевания не одобрены никакие передовые методы лечения.

Опираясь на статус BTD, в котором Nipocalimab является первым и единственным терапевтическим средством, полученным для SjD, статус FTD также предназначен для ускорения доставки новых терапевтических средств пациентам путем содействия разработке и ускорения обзора препаратов, которые демонстрируют потенциал для лечения серьезных состояний и помогают решать неудовлетворенные потребности в серьезных или опасных для жизни состояниях.
«Это знаменует собой еще один важный шаг вперед в наших усилиях по достижению значимых успехов для людей, живущих с болезнью Шегрена, серьезным и изнурительным заболеванием. Мы с нетерпением ждем продолжения тесного сотрудничества с FDA для продвижения клинической разработки Nipocalimab и потенциального предоставления столь необходимого варианта лечения для этого сообщества», — сказала Кэти Абузар (Katie Abouzahr), доктор медицины, вице-президент по портфелю аутоантител и руководитель направления заболеваний матери и плода компании Johnson & Johnson Innovative Medicine.
Не существует одобренных FDA методов лечения, которые напрямую устраняют основные причины этого сложного заболевания, связанного с серьезными последствиями для здоровья, включая хроническую сухость желез, вырабатывающих влагу, что может привести к системным осложнениям, таким как боль в суставах, усталость и воспаление в нескольких системах органов. Эти осложнения могут привести к повышенному риску смертности и другим проблемам, включая в 20 раз более высокий риск развития В-клеточных лимфом сравнительно с общей популяцией.

Исследование DAHLIAS фазы 2, результаты которого были описаны в прошлом году, представило первые в истории положительные результаты исследуемого блокатора FcRn в качестве потенциальной таргетной терапии при болезни Шегрена. Исследование достигло первичной конечной точки в группе Nipocalimab 15 мг/кг, показав относительное среднее улучшение системной активности заболевания более чем на 70% на 24-й неделе по сравнению с плацебо и снижение IgG более чем на 77%. Тенденции улучшения также наблюдались по нескольким вторичным конечным точкам. Безопасность и переносимость соответствовали другим клиническим исследованиям Nipocalimab.
О болезни Шегрена
Болезнь Шегрена является одним из наиболее распространенных заболеваний, вызванных аутоантителами, для которого в настоящее время отсутствуют методы, лечащие основную и системную природу заболевания. Это хроническое аутоиммунное заболевание, которое, по оценкам, поражает приблизительно 4 миллиона человек во всем мире и в 9 раз чаще встречается у женщин, чем у мужчин. Болезнь Шегрена характеризуется выработкой аутоантител, хроническим воспалением и лимфоцитарной инфильтрацией экзокринных желез.
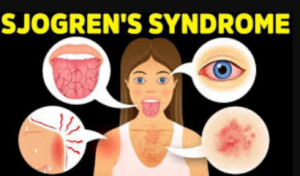
Большинство пациентов страдают от сухости слизистых оболочек (глаз, рта, влагалища), боли в суставах и усталости. Более 50% пациентов страдают от умеренной или тяжелой формы заболевания, а бремя болезни может быть таким же высоким, как при ревматоидном артрите или системной красной волчанке. Обычно это связано с ухудшением качества жизни и функциональных возможностей.
О препарате Nipocalimab
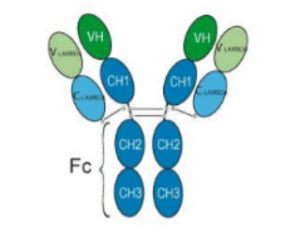
Nipocalimab — это исследуемое моноклональное антитело, разработанное для связывания с высокой аффинностью для блокирования FcRn и снижения уровней циркулирующих антител иммуноглобулина G (IgG) потенциально без влияния на другие иммунные функции. Сюда входят аутоантитела и аллоантитела, которые лежат в основе множества состояний в трех ключевых сегментах пространства аутоантител, включая редкие заболевания аутоантител, материнские заболевания плода, опосредованные материнскими аллоантителами, и ревматические заболевания. Блокада связывания IgG с FcRn в плаценте также, как полагают, ограничивает трансплацентарную передачу материнских аллоантител плоду.
Управление по контролю за продуктами и лекарствами США (FDA) и Европейское агентство по лекарственным средствам (EMA) предоставили Nipocalimab целый ряд ключевых обозначений, среди основных – Fast Track designation, статус Orphan drug, Breakthrough Therapy designation, Priority Review и некоторые другие.
О компании Johnson & Johnson
Johnson & Johnson (J&J) — американская многонациональная фармацевтическая, биотехнологическая и медицинская корпорация со штаб-квартирой в Нью-Брансуике, штат Нью-Джерси, акции которой публично торгуются на Нью-Йоркской фондовой бирже. Ее обыкновенные акции являются компонентом индекса Dow Jones Industrial Average, а компания занимает 40-е место в списке крупнейших корпораций США Fortune 500 2023 года. В 2023 году компания также заняла 40-е место в рейтинге Forbes Global 2000. В Johnson & Johnson работает около 130 000 человек по всему миру, которыми руководит нынешний председатель и главный исполнительный директор компании Хоакин Дуато (Joaquin Duato).
Johnson & Johnson была основана в 1886 году тремя братьями: Робертом Вудом Джонсоном, Джеймсом Вудом Джонсоном и Эдвардом Мидом Джонсоном, которые продавали готовые к использованию стерильные хирургические повязки. В 2023 году компания выделила свой сектор потребительского здравоохранения в новую публичную компанию Kenvue. Компания занимается исключительно разработкой и производством фармацевтических рецептурных препаратов и технологий медицинских устройств.
Johnson & Johnson — одна из самых дорогих компаний в мире и одна из двух компаний, базирующихся в США, имеющих высший кредитный рейтинг AAA.
Источник: https://www.prnewswire.com/
Источник: https://finance.yahoo.com/
21.03.2025