Клеточная терапия фокальной эпилепсии демонстрирует эффективность у первой группы пациентов
Американская биотехнологическая компания Neurona Therapeutics, Inc. сообщает, что у первого из двух пациентов, проходивших лечение препаратом NRTX-1001 в рамках КИ фазы 1/2 (NCT05135091), удалось сохранить снижение приступов более, чем на 95% по истечении 16 месяцев после начала лечения. Таким образом, инновационность исследований, проводимых Neurona Therapeutics, заключается в создании препаратов, способных бороться с лекарственно-устойчивой эпилепсией.

Аллогенная регенеративная нервно-клеточная терапия NRTX-1001 оценивается для лечения лекарственно-резистентной мезиальной височной эпилепсии (mesial temporal lobe epilepsy, MTLE). Согласно сообщению компании, набор пациентов в первую группу завершен.
Отмечено, что на исходном уровне у первого пациента, 26-летнего мужчины, в течение последних 7 лет наблюдались судороги, а за 6 месяцев до начала клеточной терапии, наблюдалось в среднем, 32 приступа в месяц. В первой группе пациентов лечат с помощью однократной, более низкой дозы NRTX-1001 и годового режима иммуносупрессивной терапии, предназначенного для облегчения интеграции и устойчивости клеточной терапии. Всего в группу было включено 5 пациентов, и все 5 получали NRTX-1001.
Второй пациент, проходивший лечение и наблюдавшийся в течение 12 месяцев после приема NRTX-1001, также продемонстрировал снижение приступов более чем на 95%. Кроме того, Neurona Therapeutics отметила, что у этого пациента не было никаких приступов в течение 6 месяцев. Сообщается, что на исходном уровне у этой пациентки, 59-летней женщины, в течение последних 9 лет наблюдались судороги, а за 6 месяцев до начала клеточной терапии, в среднем, возникало 14 приступов ежемесячно.
Neurona сообщает, что у этих двух пациентов нейрокогнитивное тестирование по протоколу, проведенное как на исходном уровне, так и после лечения NRTX-1001, выявило потенциальное улучшение памяти за счет увеличения баллов по подмножеству пунктов, измеряемых с помощью тестов. С точки зрения безопасности не было обнаружено никаких изменений. Серьезные или тяжелые нежелательные явления зарегистрированы у любого из 5 пациентов, проходивших лечение.
«Первые данные нашего текущего открытого клинического исследования фазы 1/2 на сегодняшний день являются многообещающими, демонстрируя, что NRTX-1001 до сих пор хорошо переносится и может привести к существенному и длительному уменьшению приступов у пациентов с лекарственно-устойчивой мезиальной височной болезнью. долевой эпилепсии», — заявил Кори Р. Николас (Cory R. Nicholas), PhD, генеральный директор Neurona. «Видеть, что данные продолжают сохраняться в течение долгосрочных 12 с лишним месяцев наблюдения за первыми двумя субъектами, чрезвычайно полезно. Мы с нетерпением ждем возможности набрать нашу вторую группу из пяти человек и продолжить разработку этой потенциально преобразующей терапии для людей, живущих с лекарственно-устойчивой эпилепсией».
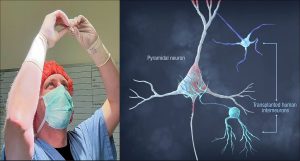
NRTX-1001 состоит из человеческих интернейронов, которые обеспечивают долговременную секрецию гамма-аминомасляной кислоты, тормозного нейротрансмиттера. Последний, как ожидается, восстанавливает нейронные сети. Участники КИ получают NRTX-1001 посредством однократного стереотаксического внутримозгового введения. В ходе исследования доказательства жизнеспособности нервных клеток и местного воспаления будут оцениваться с помощью МРТ в течение 2 лет после трансплантации.
«Прекращение первым пациентом в КИ иммуносупрессивной терапии с продолжающимся >95% снижением общего количества ежемесячных приступов говорит о перспективности этого лечения», — добавил Дэвид Блюм (David Blum), доктор медицины, главный медицинский директор Neurona. «Второй субъект получавший однократную дозу NRTX-1001 и достигший конечной точки через 1 год, также продолжает хорошо себя чувствовать с уменьшением приступов >95%, и он не вообще сообщал о приступах в течение последних 6 месяцев. Мы ожидаем обновления информации о прогрессе этих двух пациентов и предоставления данных о дополнительных пациентах из этой первой группы в IV квартале 2023 года».
Отметим, что NRTX-1001 — не единственный разрабатываемый современный препарат для лечения MTLE. В сентябре 2023 года AMT-260 компании uniQure NV, исследуемая генная терапия на основе вектора аденоассоциированного вируса (AAV), предназначенная для лечения рефрактерной MTLE, получила разрешение FDA на применение нового исследуемого препарата. AMT-260 состоит из 2 спроектированных микроРНК, доставленных локально в векторе AAV9. Они предназначены для деградации GRIK2, гена, участвующего в выработке подтипа GLUK2 глутаматного рецептора. Компания планирует начать скрининговую деятельность по оценке AMT-260 в КИ фазы 1/2а до конца года.
О клиническом исследовании NRTX-1001 при лечении мезиальной височной эпилепсии (MTLE)
Клиническое исследование NCT05135091 предназначено для оценки безопасности и эффективности однократного введения NRTX-1001 при лекарственно-устойчивом MTLE. Первый этап исследования представляет собой открытое исследование с увеличением дозы с участием до 10 человек с MTLE, при этом 5 пациентов будут получать лечение в начальной дозе, а 5 – в более высокой дозе. Пациенты, получающие однократную инфузию клеток NRTX-1001, будут контролироваться на предмет безопасности, переносимости и влияния на симптомы эпилепсии. Набор пациентов продолжается в центрах эпилепсии по всей территории США. Первая часть КИ поддерживается грантом в размере $8 млн от Калифорнийского института регенеративной медицины (California Institute for Regenerative Medicine, CIRM; CLIN2-13355).

О NRTX-1001
NRTX-1001 является кандидатом на регенеративную терапию нервных клеток, полученным из плюрипотентных стволовых клеток человека. Полностью дифференцированные нервные клетки, называемые интернейронами, секретируют тормозной нейромедиатор гамма-аминомасляную кислоту (ГАМК). Вводимые в виде однократной дозы интернейроны человека предназначены для интеграции и иннервации цели, а также для длительного подавления судорожной активности в эпилептической области мозга. NRTX-1001 производится на собственном предприятии Neurona, отвечающем требованиям GMP, с использованием запатентованных методов. Интернейроны NRTX-1001 криоконсервируются и отправляются в клинические центры для использования в качестве аллогенной, готовой исследовательской терапии.
О мезиальной височной эпилепсии (MTLE)
По данным Центров по контролю и профилактике заболеваний (Centers for Disease Control and Prevention), около 3,4 миллиона американцев страдают эпилепсией, и от 25 до 35% живут с продолжающимися припадками, несмотря на лечение одобренными лекарствами, что иллюстрирует огромные неудовлетворенные медицинские потребности в этом сообществе. MTLE является распространенным типом фокальной эпилепсии у взрослых, и, в первую очередь, поражает внутренние структуры височной доли, где припадки часто начинаются в структуре, называемой гиппокампом. Для людей с судорогами, резистентными к противосудорожным препаратам, вариантом может быть хирургическое вмешательство при эпилепсии, при котором поврежденная височная доля удаляется хирургическим путем либо подвергается лазерной абляции. Однако современные хирургические методы доступны и эффективны не для всех пациентов, они разрушают ткани и могут иметь значительные побочные эффекты.
О Neurona Therapeutics, Inc.
Neurona сосредоточена на разработке кандидатов на регенеративную клеточную терапию, обладающих лечебным потенциалом при однократном приеме. Она разрабатывает готовые кандидаты на аллогенную терапию нервных клеток, предназначенные для обеспечения долгосрочного восстановления дисфункциональных нейронных сетей при множественных неврологических расстройствах. Компания, созданная в 2008 году, имеет штаб-квартиру в Сан-Франциско (Калифорния, США), ее состав – примерно 100 высококвалифицированных специалистов. В 2015 году Neurona объявила о своем запуске, получив финансирование серии А в размере $23,5 млн под руководством The Column Group.
Источник: https://www.cgtlive.com/
Источник: https://www.neuronatherapeutics.com/
Источник: https://golden.com/
25.10.2023