«Мягкий» CRISPR предлагает новый подход к генетическим дефектам
Лечение изнурительных генетических заболеваний является одной из самых сложных задач современной медицины. За последнее десятилетие развитие технологий CRISPR и достижения в области генетических исследований дали новую надежду пациентам и их семьям, хотя безопасность этих новых методов по-прежнему вызывает серьезную озабоченность. В публикации от 1 июля в журнале Science Advances группа биологов из Калифорнийского университета в Сан-Диего, в которую входят ученый с докторской степенью Ситара Рой, специалист Аннабель Гишар и профессор Итан Бир, описывает новый, более безопасный подход, который может исправить генетические дефекты в будущем.

Их стратегия, использующая естественный механизм репарации ДНК, обеспечивает основу для новых стратегий генной терапии, способных вылечить широкий спектр генетических заболеваний . Во многих случаях люди, страдающие от генетических нарушений, несут различные мутации в двух копиях генов, унаследованных от родителей. Это означает, что часто мутация на одной хромосоме будет иметь аналог функциональной последовательности на другой хромосоме.
Исследователи использовали инструменты генетического редактирования CRISPR, чтобы использовать этот факт. «Здоровый вариант может быть использован механизмом репарации клетки для исправления дефектной мутации после вырезания мутантной ДНК, — сказал Гишар, старший автор исследования.» Работая с плодовыми мушками, исследователи создали мутантов, позволяющих визуализировать такое «репарирование по шаблону гомологичной хромосомы» или HTR, путем производства пигментов в их глазах. Такие мутанты изначально имели полностью белые глаза. Но когда те же мухи экспрессировали компоненты CRISPR (направляющая РНК плюс Cas9), у них появлялись большие красные пятна на глазах, что служило признаком того, что механизму репарации ДНК клетки удалось обратить мутацию, используя функциональную ДНК из другой хромосомы.
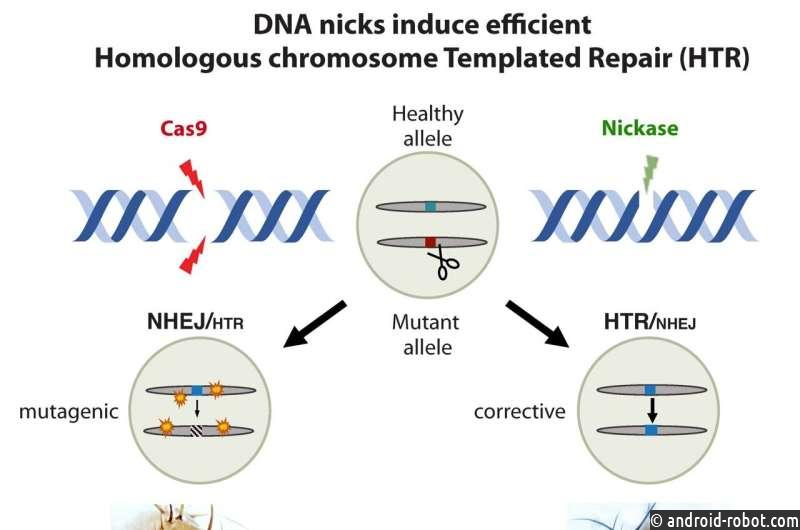
Затем они протестировали свою новую систему с вариантами Cas9, известными как «никазы», которые нацелены только на одну цепь ДНК, а не на обе. Удивительно, но авторы обнаружили, что такие порезы также приводили к высокому уровню восстановления красного цвета глаз почти наравне с нормальными (не мутировавшими) здоровыми мухами. Они обнаружили 50-70% успешности восстановления с помощью никазы по сравнению с 20-30% при двухцепочечном разрезе Cas9, который также вызывает частые мутации и нацелен на другие участки генома (так называемые нецелевые мутации). «Я не мог поверить, насколько хорошо сработала никаза — это было совершенно неожиданно», — сказал Рой, ведущий автор исследования. Исследователи отметили, что универсальность новой системы может служить моделью для исправления генетических мутаций у млекопитающих.
«Мы пока не знаем, как этот процесс будет транслироваться в клетки человека и сможем ли мы применить его к любому гену», — сказал Гишар. «Может потребоваться некоторая корректировка для получения эффективного HTR для вызывающих болезни мутаций, переносимых человеческими хромосомами».
Новое исследование расширяет предыдущие достижения группы в области точного редактирования с помощью «аллельных драйвов», которые расширяют принципы генных драйвов с направляющей РНК, которая направляет систему CRISPR на вырезание нежелательных вариантов гена и замену их предпочтительной версией.
Ключевой особенностью исследования команды является то, что их система на основе никазы вызывает гораздо меньше целевых и нецелевых мутаций, что, как известно, происходит с более традиционными изменениями CRISPR на основе Cas9. Они также говорят, что медленная непрерывная доставка компонентов никазы в течение нескольких дней может оказаться более выгодной, чем разовая доставка.
«Еще одним заметным преимуществом этого подхода является его простота», — сказал Бир. «Он основан на очень небольшом количестве компонентов, а разрывы ДНК «мягкие», в отличие от Cas9, который производит полные разрывы ДНК, часто сопровождаемые мутациями». «Если бы частоту таких событий можно было увеличить либо за счет стимуляции межгомологического спаривания, либо за счет оптимизации процессов репарации, специфичных для ник, такие стратегии можно было бы использовать для коррекции многочисленных доминантных или трансгетерозиготных мутаций, вызывающих заболевание», — сказал Рой.
Источник: https://android-robot.com/
4.07.2022