Pfizer и Astellas получили статус Priority Review для комбинированной терапии Padcev при мышечно-инвазивном раке мочевого пузыря
FDA предоставило Pfizer и Astellas право на приоритетное рассмотрение дополнительной заявки для получения лицензии на биологический препарат (sBLA) для периоперационного применения Padcev (enfortumab vedotin-ejfv) в комбинации с ингибитором PD-1 Keytruda (pembrolizumab) при мышечно-инвазивном раке мочевого пузыря (МИРМП).

Цель заявки – получить разрешение на использование этой комбинированной терапии для всех пациентов с МИРМП, независимо от возможности применения цисплатина. Это потенциально может расширить область применения комбинации, которая ранее ограничивалась случаями, когда лечение цисплатином не представлялось возможным. FDA установило целевую дату принятия решения на 17 августа 2026 года.
Заявка была основана на данных клинического исследования III фазы EV-304 (KEYNOTE-B15), изучающего периоперационное применение enfortumab vedotin и pembrolizumab у пациентов, которым подходит химиотерапия на основе cisplatin.
Данные исследования EV-304 показали снижение риска рецидива опухоли, прогрессирования заболевания или смерти на 47%, а также снижение риска смерти на 35% по сравнению со стандартной неоадъювантной химиотерапией gemcitabine и cisplatin.
Частота патологически полного ответа (pCR) составила 55,8% для комбинированной терапии против 32,5% в группе химиотерапии.
Профиль безопасности комбинированной терапии соответствовал предыдущему опыту, новых сигналов безопасности не наблюдалось. Обсуждения с другими международными органами здравоохранения относительно потенциальной подачи заявок на регистрацию продолжаются.
Участники получали либо периоперационную терапию enfortumab vedotin и pembrolizumab, либо неоадъювантную химиотерапию, при этом в обеих группах проводилось хирургическое вмешательство. Первичной конечной точкой является выживаемость без событий (event-free survival, EFS), а ключевыми вторичными конечными точками — общая выживаемость (overall survival, OS) и частота pCR.
Главный онколог компании Pfizer Джефф Легос (Jeff Legos) заявил: «Для людей с мышечно-инвазивным раком мочевого пузыря операция часто является лишь началом долгого и неопределенного пути, и слишком многие пациенты сталкиваются с рецидивом заболевания. В случае одобрения, периоперационная терапия PADCEV® в сочетании с pembrolizumab может существенно изменить этот опыт, потенциально помогая пациентам снизить риск рецидива и продлить жизнь, независимо от того, подходит ли им лечение цисплатином».
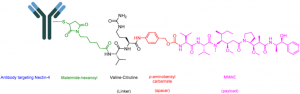
О препарате PADCEV®
PADCEV® (enfortumab vedotin) — рецептурный препарат, используемый для лечения взрослых с уротелиальным раком (рак мочевого пузыря и рак мочевыводящих путей, таких как почечная лоханка, мочеточник или уретра). Он разработан как конъюгат антитела с лекарственным препаратом (ADC), который непосредственно воздействует на раковые клетки и уничтожает их. Часто используется при запущенном, метастатическом или мышечно-инвазивном раке мочевого пузыря.
Первая линия лечения (запущенный рак): в сочетании с Keytruda (pembrolizumab) для взрослых с местно-распространенным или метастатическим уротелиальным раком (мУР). Инвазивный рак мочевого пузыря (ИРМП): применяется в комбинации с pembrolizumab у пациентов, которым противопоказана химиотерапия цисплатином, и у которых выявлен инвазивный рак мочевого пузыря. В качестве монотерапии применяется у пациентов с местнораспространенным или метастатическим уротелиальным раком, которые ранее получали ингибитор PD-1/PD-L1 и химиотерапию на основе препаратов платины, или которые не могут получать цисплатин и прошли как минимум одну предшествующую терапию.
Источник: https://www.pharmaceutical-technology.com/
Источник: https://www.curetoday.com/
22.04.2026