Препарат Datroway от AstraZeneca и Daiichi Sankyo получил ускоренное одобрение FDA для лечения рака легких
Препарат Datroway (datopotamab deruxtecan) совместной разработки фармгигантов AstraZeneca (AZ) и Daiichi Sankyo получил ускоренное одобрение (Accelerated Approval Program) от Управления по контролю за продуктами и лекарствами США (FDA) для лечения подгруппы пациентов с немелкоклеточным раком легких (НМРЛ).

Datroway относится к относительно новому классу противораковых препаратов, которые сочетают селективность антител с мощным клеточно-уничтожающим действием химиотерапии или других противораковых агентов.
Datroway представляет собой коньюгат (комбинация) – сложную структуру и состоит из двух, соединенных между собой частей. АНТИТЕЛО – это белок, разработанный так, чтобы напоминать естественные антитела организма, которые иммунная система вырабатывает для борьбы с инфекциями и вредными веществами. Антитело нацеливается и прикрепляется к определенному белку, обнаруженному в раковых клетках. В случае Datroway оно прикрепляется к белку Trop-2. ЛЕКАРСТВО – это химическое вещество, которое антитело выделяет для атаки и уничтожения раковых клеток.
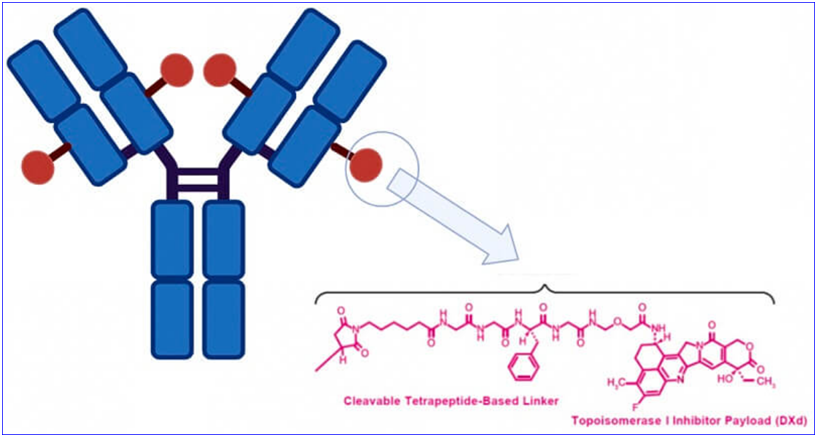
Конъюгат антитела и препарата был одобрен для использования у взрослых с местнораспространенным или метастатическим мутированным EGFR НМРЛ, которые ранее получали терапию, направленную на EGFR, и химиотерапию на основе платины, что делает его первой и единственной терапией, направленной на TROP2, одобренной в США для лечения рака легких.
Решение FDA по препарату было основано на положительных результатах анализа подгруппы исследования TROPION-Lung05 на средней стадии и подкреплено данными исследования TROPION-Lung01 на поздней стадии.
В исследованиях Datroway показал подтвержденный объективный уровень ответа 45% у пациентов с ранее леченным местнораспространенным или метастатическим EGFR-мутированным НМРЛ. Полные ответы и частичные ответы наблюдались у 4,4% и 40% пациентов соответственно, а медианная продолжительность ответа составила 6,5 месяцев.
В соответствии с ускоренным путем одобрения FDA, дальнейшее одобрение этого показания может зависеть от проверки и описания клинической пользы в подтверждающем исследовании.
Американское онкологическое общество подсчитало, что в этом году в США рак легких будет диагностирован примерно у 226 650 человек, при этом НМРЛ составит около 87% случаев. Для 10–15% пациентов с НМРЛ в США, имеющих мутацию EGFR, установленная терапия первой линии в метастатической обстановке включает терапию, направленную на EGFR, с химиотерапией на основе платины или без нее. Однако у большинства пациентов в конечном итоге наступит прогрессирование заболевания, и им потребуется последующая терапия.
Препарат, который уже одобрен в США для лечения некоторых случаев рака молочной железы, был открыт Daiichi Sankyo и совместно разрабатывается и выводится на рынок AstraZeneca и Daiichi Sankyo.
Дейв Фредриксон (Dave Fredrickson), исполнительный вице-президент подразделения онкологической гематологии в Аризоне, сказал: «Это первое одобрение препарата Datroway для лечения рака легких обеспечивает столь необходимую возможность для пациентов с запущенным раком легких с мутацией EGFR, чье заболевание стало устойчивым к предыдущим методам лечения, независимо от вызвавшей его мутации».
Программа ускоренного одобрения FDA
Программа ускоренного одобрения FDA (FDA’s Accelerated Approval Program) позволяет более раннее одобрение лекарств, которые лечат серьезные или опасные для жизни состояния и заполняют неудовлетворенную медицинскую потребность, на основе первоначальных доказательств, таких как суррогатные конечные точки, которые с достаточной вероятностью предскажут клиническую пользу. Эта программа предназначена для ускорения доступа к потенциально полезным методам лечения, пока продолжаются подтверждающие испытания для проверки клинической пользы.
О компании AstraZeneca
AstraZeneca — британо-шведская фармацевтическая компания, зарегистрированная в Великобритании. Основана 6 апреля 1999 г., штаб-квартира расположена в Кембридже, Великобритания. Постоянно входит в мировую десятку по объёму продаж рецептурных препаратов. Генеральный директор: Pascal Soriot (1 окт. 2012 г.). Дочерние компании: Alexion Pharmaceuticals, EsoBiotec B.V. и др.
О компании AstraZeneca
Daiichi Sankyo — это глобальная фармацевтическая компания со штаб-квартирой в Токио, Япония, с присутствием в более чем 20 странах. Она известна разработкой и маркетингом важных инновационных лекарств, в частности, в области онкологии и сердечно-сосудистых заболеваний. Daiichi Sankyo образована в 2006 году путем слияния двух известных японских компаний Daiichi и Sankyo.
Источник: https://pmlive.com/
Источник https://datroway.com/
Источник: https://www.pharmaceutical-technology.com/
25.06.2025