Тестирование эффективности противоопухолевых антиангиогенных препаратов на модели ксенографта
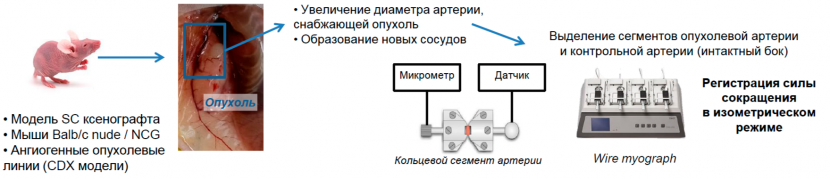
Краткое описание дизайна исследования
Иммунодефицитным мышам перевивают подкожно целевую ангиогенную опухолевую линию. После достижения опухолью целевого объема, мышей рандомизируют по группам так, чтобы средний объем опухоли во всех группах не отличался, затем проводят введение испытуемых веществ, прижизненное измерение объема опухоли с оценкой противоопухолевого действия (расчет ТРО). После окончания периода введения мышей эвтаназируют, проводят макроскопическую оценку артерий, снабжающих опухоли, и контрольных артерий с противоположной стороны. Выделяют артерии и делят на кольцевые сегменты длиной 2 мм. Каждый сегмент помещают в на 2 проволоки в камере wire myograph, где определяют их диаметр и регистрируют сокращение или расслабление в изометрическом режиме в ответ на добавление различных агонистов.
Определяемые параметры:
- Диаметр артерий
- Сокращение в ответ на агонисты адренорецепторов, серотонин, тромбоксан А2 (и проч.)
- Расслабление (эндотелий-зависимое, эндотелий-независимое)
Пример результатов исследования (зависимость силы сокращения контрольной артерии и артерии, снабжающей опухоль, от концентрации агонистов)
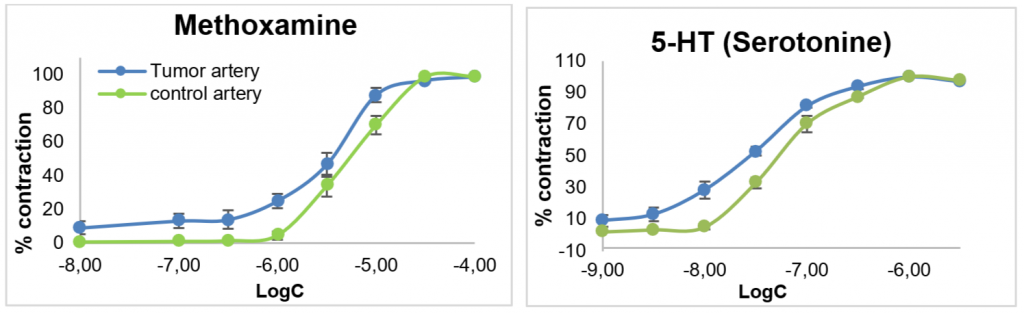
Для снабжающих опухоли артерий характерна более высокая реактивность на серотонин и агонист α1-адренорецепторов метоксамин
Tumor — это артерия, которая ведет к опухоли (новообразованная).
Control — это симметричная артерия с той стороны, где нет опухоли.
Было показано увеличение чувствительности опухолевых артерий на агонист α1-адренорецепторов метоксамин и агонист серотониновых (5-HT) рецепторов. Изменение серотонинового сигналинга согласуется с последними литературными данными о модуляции серотониновой оси внутри некоторых опухолей (https://pubmed.ncbi.nlm.nih.gov/40403728/).
Также было подтверждено отличие в размерах сосудов: артерия, ведущая к опухоли, значительно больше симметричной. Диаметр контрольной артерии составил в среднем 177 мкм, диаметр опухолевой — 200 мкм.
Изменение диаметра и тонус снабжающих опухоли артерий могут влиять на доставку препарата в опухоль, и, следовательно, на его эффективность (https://pubmed.ncbi.nlm.nih.gov/15126361/; https://www.frontiersin.org/journals/pharmacology/articles/10.3389/fphar.2017.00952/full ).
Таким образом, влияние исследуемого препарата/комбинаций препаратов на диаметр и/или регуляцию тонуса артерий может быть одним из способов оценки эффективности тест-объектов в доклинических исследованиях.
Данное тестирование может выполняться как самостоятельное или дополнять классическое исследование противоопухолевой активности в модели ксенографтов.