В ЕС рекомендовали разрешить таблетки Paxlovid для лечения COVID-19
Комитет EMA по лекарственным средствам для человека (CHMP) рекомендовал предоставить условное регистрационное удостоверение для перорального противовирусного препарата Paxlovid (Паксловид, PF-07321332/ритонавир) для лечения COVID-19.
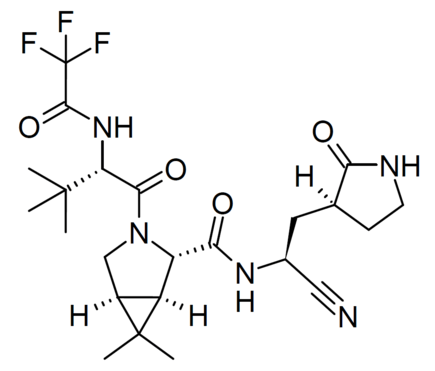
Заявителем является Pfizer Europe MA EEIG. Комитет рекомендовал разрешить Paxlovid для лечения COVID-19 у взрослых, которым не требуется дополнительный кислород и повышен риск развития тяжелой формы заболевания. Paxlovid — первое пероральное противовирусное лекарство, рекомендованное в ЕС для лечения COVID-19. Он содержит два активных вещества, PF-07321332 (нирматрелвир) и ритонавир, в двух разных таблетках. PF-07321332 работает за счет снижения способности SARS-CoV-2 (вируса, вызывающего COVID-19) размножаться в организме, в то время как ритонавир продлевает действие PF-07321332, позволяя ему дольше оставаться в организме на уровнях, которые влияют на размножение вируса. CHMP проанализировал данные клинического исследования с участием пациентов с COVID-19, показывающие, что лечение Paxlovid значительно снижает количество госпитализаций или смертей у пациентов, у которых есть хотя бы одно основное заболевание, подвергающее их риску тяжелого течения COVID-19. Анализ проводился у пациентов, получавших Paxlovid или плацебо (фиктивное лечение) в течение 5 дней после появления симптомов COVID-19 и тех, которые не получали и не должны были получать лечение антителами. В течение месяца после лечения частота госпитализаций или летальных исходов составила 0,8% (8 из 1039) для пациентов, получавших Paxlovid, сравненительно с 6,3% (66 из 1046) для тех, кто получал плацебо. В группе Paxlovid летальных исходов не было, а в группе плацебо — 12 смертей. Большинство пациентов в исследовании были инфицированы дельта-вариантом. Основываясь на лабораторных исследованиях, ожидается, что Paxlovid также будет активен против Омикрона и других вариантов. Профиль безопасности Paxlovid был благоприятным, а побочные эффекты в целом были легкими. Однако известно, что ритонавир влияет на действие многих других лекарств, и предупреждения и рекомендации были включены в информацию о продукте. Кроме того, компания разместила на своем веб-сайте инструмент взаимодействия с лекарственными средствами, доступ к которому можно получить с помощью QR-кода, включенного в информацию о продукте и на внешней упаковке. В соответствующие организации медицинских работников будет отправлено письмо, чтобы напомнить им об этой проблеме. CHMP пришел к выводу, что польза от лекарства превышает его риски для утвержденного использования, и теперь направит свои рекомендации в Европейскую комиссию для быстрого принятия решения, применимого во всех государствах-членах ЕС. Европейская комиссия теперь ускорит процесс принятия решения о выдаче решения об условном разрешении на продажу Paxlovid, что позволит продавать это лекарство на территории ЕС. Условное регистрационное удостоверение (CMA) используется в качестве ускоренной процедуры авторизации для ускорения утверждения лекарственных средств во время чрезвычайных ситуаций в области общественного здравоохранения в ЕС. CMA позволяют разрешать лекарства, которые удовлетворяют неудовлетворенные медицинские потребности, на основе менее полных данных, чем обычно требуются. Это происходит, если польза от непосредственной доступности лекарства для пациентов перевешивает риск, связанный с тем, что еще не все данные доступны. CMA гарантирует, что одобренное лекарство соответствует строгим стандартам ЕС по эффективности, безопасности и качеству и производится на утвержденных, сертифицированных предприятиях в соответствии с высокими фармацевтическими стандартами для крупномасштабного производства.
31.01.2022