Исследование ин витро проницаемости в тесте Caco-2 для биовейвера, основанного на биофармацевтической системе классификации (БКС), тесты на растворимость, стабильность и ин витро проницаемость в модели Сасо2/Pgp
Биовейвер — процедура оценки биоэквивалентности лекарственного препарата без проведения исследования биоэквивалентности in vivo в соответствии с определением Решения Совета ЕЭК N 85 (Приложение № 4 к Правилам проведения исследований биоэквивалентности ЛП в рамках Евразийского экономического союза) и руководством ICH M9 guideline on biopharmaceutics classification system-based biowaivers.
Проведение исследования в тесте Сасо2 для биовейвера, основанного на биофармацевтической системе классификации (БКС) в исследовательском центре Химрар
Критерии отнесения к классам БКС:
I класс
(Парацетамол) |
III класс
(Циметидин) |
II класс
(Ибупрофен) |
IV класс
(Фуросемид) |
Растворимость. Исследование профиля pH-растворимости действующего вещества для биовейвера, основанного на биофармацевтической системе классификации (БКС).
Для этого требуется провести исследование не менее чем с 3 буферными растворами с различными pH, находящимся в вышеуказанном диапазоне (предпочтительно при pH 1,2; 4,5 и 6,8) и, по возможности, при pKa, если pKa находится в указанном диапазоне pH.
Используется метод встряхивания флакона (shake-flask) или другой подходящий.
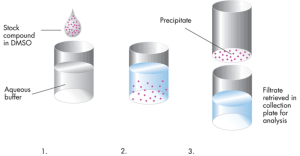
Действующее вещество признается хорошо растворимым, если его максимальная однократная доза полностью растворяется в 250 мл буферного раствора в диапазоне pH от 1 до 6,8.
Всасывание (проникающая способность). Исследование кишечной проницаемости в модели Caco-2 ин витро для биовейвера, основанного на биофармацевтической системе классификации (БКС).
Исследования проводятся с целью подтвердить полную абсорбцию действующего вещества у человека (абсорбцию более 85%). Полное всасывание обычно обусловлено высокой проникающей способностью действующего вещества через кишечный барьер. В качестве обоснования используют результаты исследований абсолютной биодоступности или материального баланса. Для оценки проводят исследование в тесте сасо2.
Тест кишечной проницаемости в модели Сасо-2 (пассивная проницаемость и активный транспорт)
Тест-система для определение клеточной проницаемости и активного транспорта на модели Caco-2 с PGP используется для исследований транспорта через клеточный монослой. Клетки карциномы кишечника Caco-2 морфологически и функционально похожи на барьерный эпителий кишечника и успешно применяются для оценки проницаемости и абсорбции в ЖКТ. Caco-2 клетки также имеют ряд транспортеров, включая P-гликопротеин (Pgp), и используются для изучения активного транспорта веществ. Исследование проводится в прямом (А-В) и обратном (В-А) направлении, оценивая показатель проницаемости и эффлюкс-отношение проницаемости
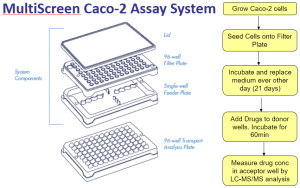
Метод входит в панель тестов ADME (Absorption, Distribution, Metabolism, Excretion) и является общепризнанным методом оценки кишечной проницаемости in vitro, а также тестом, по результатам которого возможно установить проницаемость по биофармацевтической классификационной системе (БКС) путём сравнения с контрольными веществами.
Исследование стабильности в желудочно-кишечном тракте ин витро
Стабильность в желудочно-кишечном тракте может быть исследована с использованием модельных желудочных и кишечных жидкостей: тест на определение стабильности в искусственном желудочном и кишечном соке (описание метода). Значительная деградация (>10%) лекарственного вещества исключает классификацию по БКС.
Изучение всасывания (проникающей способности) проводится в соответствии с ICH M9 guideline on biopharmaceutics classification system-based biowaivers
О лаборатории:
Лаборатория биоаналитики исследовательского центра ХимРар имеет многолетний опыт в проведении исследований для определения класса БКС и прохождения процедуры биовейвера, штат квалифицированных специалистов и современный парк аналитического оборудования. Команда центра разработает дизайн ин витро исследований для прохождения биовейвера, включая исследования: растворимости, всасывание (проникающая способность), оценку результатов теста.
Используемое аналитическое оборудование:
Agilent 1290 Infinity + AB Sciex 5500 QTRAP Agilent 1260 Infinity, cистемы высокоэффективной жидкостной хроматографии с УФ- детекторами, рефрактометрическим детектором и ELSD-детектором, УФ-спектрофотометры, тестеры растворения, данное оборудование помогает выполнять широкий спектр задач. Оборудования проходит своевременную поверку и сервисное обслуживания.
- Возможность проведения исследования, доступность других доклинических тестов можно уточнить отправив запрос на email: sa@chemrar.ru

О биовейвере на основе БКС:
Биовейвер, основанный на биофармацевтической системе классификации (БКС), направлен на уменьшение количества исследований и может служить заменой биоэквивалентности in vivo. Процедура сокращает время регистрации лекарственных препаратов, избежать проведения клинических исследований и возможных рисков для пациентов.
БКС разделяет лекарственные препараты на основе их растворимости в воде и проницаемости через клеточные мембраны. В соответствии с БКС, препараты делятся на четыре класса. В случае, когда лекарственный препарат относится к классу I или классу III по BCS, и существуют сравнимые препараты уже зарегистрированы, можно применить биовейвер. Это означает, что проведения клинических исследований на человеке можно избежать, поскольку биоэквивалентность или терапевтическая эквивалентность могут быть обоснованы с использованием результатов ранее проведенных исследований аналогичных препаратов.
Биовейвер возможен для ЛП для приема внутрь в твердых ЛФ системного действия с немедленным высвобождением, включая комбинированные ЛФ, лекарственных форм, диспергирующихся в полости рта, если исключена абсорбция из полости рта, если исследуемый и референтный лекарственные препараты содержат одинаковые действующие вещества, различные соли при условии их принадлежности к I и III классу по БКС (высокая растворимость и предсказуемая абсорбция).
Если исследуемый лекарственный препарат содержит сложные эфиры, стереоизомеры и их смеси, комплексы или производные действующего вещества референтного лекарственного препарата, биовейвер невозможен, поскольку различия могут привести к различной биодоступности, не выявляемой с помощью экспериментов, используемых в концепции биовейвера, основанного на БКС.
ДЛЯ ЗАКАЗА ИССЛЕДОВАНИЙ:
Сизюхин Андрей Владимирович
Руководитель отдела продаж R&D сервисов, доклинические исследования
E-mail: sa@chemrar.ru
Тел.: +7 (495) 925-30-74 +доб.(538)